Gabrielle Fimbres
responsable de comunicación externa
520.222.4573
[email protected]
Roche recibe la aprobación de la FDA para la prueba VENTANA ALK (D5F3) CDx para identificar a los pacientes con carcinoma pulmonar aptos para recibir un tratamiento con ALECENSA (alectinib) de Roche.
Tucson (Arizona)
07 de noviembre de 2017
- La prueba VENTANA ALK (D5F3) CDx1 de companion diagnostics se indica ahora como un soporte para la identificación de los pacientes con carcinoma pulmonar aptos para recibir un tratamiento con tres fármacos únicos
- Se estima que en 2017 se diagnosticará carcinoma pulmonar a más de 222 000 estadounidenses, de los cuales, el 85 % de los casos serán carcinoma pulmonar no microcítico (CPNM)2
- La cinasa de linfoma anaplásico (anaplastic lymphoma kinase, ALK) es un importante biomarcador que se encuentra en el CPNM. Su detección e inhibición puede ayudar a reducir los tumores de algunos pacientes con ALK positivo
Roche (SIX: RO, ROG; OTCQX:RHHBY) ha anunciado hoy que ha obtenido la autorización de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) para el uso de la prueba VENTANA ALK (D5F3) CDx como companion diagnostics para identificar a los pacientes con carcinoma pulmonar no microcítico (CPNM) ALK positivos aptos para recibir un tratamiento con el fármaco de Roche ALECENSA® (alectinib). La prueba VENTANA ALK (D5F3) CDx es la única prueba que cuenta con la autorización de la FDA como companion diagnostics para el uso de ALECENSA.
Estamos muy entusiasmados con la ampliación de la ficha técnica a companion diagnostics para la prueba ALK (D5F3). Esta prueba immunohistoquímica proporcionará información crucial sobre las opciones de tratamiento para los pacientes con carcinoma pulmonar no microcítico, indicó Ann Costello, directora de Roche Tissue Diagnostics. La capacidad de identificar pacientes con ALK positivo con rapidez con una sencilla prueba IHQ garantiza que más pacientes se beneficien del tratamiento dirigido.
Varios estudios han demostrado que la prueba VENTANA ALK (D5F3) CDx permite identificar a más pacientes que podrán beneficiarse de un tratamiento dirigido contra ALK en lugar de una prueba de hibridación in situ con fluorescencia (fluorescent in situ hybridization, FISH).3,4,5,6 La prueba VENTANA ALK (D5F3) CDx está disponible para su uso con los sistemas de tinción de muestras Roche BenchMark XT o BenchMark ULTRA IHQ/HIS.7
Acerca de la prueba VENTANA ALK (D5F3) CDx
La prueba VENTANA ALK (D5F3) CDx ha sido diseñada para la detección cualitativa de la proteína cinasa de linfoma anaplásico (ALK) en tejido de carcinoma pulmonar no microcítico (CPNM) fijado en formol e incluido en parafina (FFPE) con tinción con un dispositivo automatizado BenchMark XT o BenchMark ULTRA. Su uso está indicado como soporte para la identificación de pacientes aptos para el tratamiento con XALKORI® (crizotinib), ZYKADIA® (ceritinib) o ALECENSA® (alectinib).
Este producto debe ser interpretado por un patólogo cualificado, junto con un examen histológico, información clínica pertinente y los controles adecuados.
Este producto está destinado al uso en el diagnóstico in vitro (in-vitro diagnostic, IVD). Para más información, visita ALKIHC.com.
Acerca de ALECENSA
Para más información sobre ALECENSA (alectinib), visita www.alecensa.com.
Acerca de Roche
Roche es una empresa internacional, pionera en el desarrollo de medicamentos y productos de diagnóstico para hacer avanzar la ciencia y mejorar la vida de las personas. La potencia combinada farmacéutica y diagnóstica bajo un mismo techo ha convertido a Roche en el líder de la atención sanitaria personalizada, una estrategia orientada a proporcionar a cada paciente el mejor tratamiento posible.
Roche es la mayor empresa biotecnológica del mundo, con medicamentos auténticamente diferenciados en las áreas de oncología, inmunología, enfermedades infecciosas, oftalmología y enfermedades del sistema nervioso central Roche también es líder mundial en diagnóstico in vitro y diagnóstico de cáncer basado en el tejido, y se sitúa a la vanguardia en el control de la diabetes.
Fundada en 1896, Roche busca mejores vías de prevenir, diagnosticar y tratar las enfermedades, así como de contribuir al desarrollo sostenible de la sociedad. La empresa también tiene como objetivo mejorar el acceso de los pacientes a las innovaciones médicas trabajando con todas las partes interesadas pertinentes. La lista Modelo de Medicamentos Esenciales de la Organización Mundial de la Salud contiene 30 medicamentos desarrollados por Roche, entre ellos antibacterianos que salvan vidas, antipalúdicos y antineoplásicos. Por noveno año consecutivo, Roche ha sido reconocida en los Índices de Sostenibilidad Dow Jones (DJSI) como la empresa más sostenible del grupo Industria Farmacéutica, Biotecnología y Ciencias Biológicas.
El Grupo Roche, con sede central en Basilea (Suiza), está presente operativamente en más de 100 países y en el 2016, contaba con más de 94 000 empleados en todo el mundo. Ese mismo año, Roche invirtió 9900 millones de CHF en I+D y sus ventas alcanzaron la cifra de 50 600 millones de CHF. Genentech (Estados Unidos) es un miembro de plena propiedad del Grupo Roche. Roche es el accionista mayoritario de Chugai Pharmaceutical (Japón). Para más información, visita la página www.roche.com.
VENTANA y BENCHMARK son marcas registradas de Roche. El resto de nombres de productos y marcas registradas son propiedad de sus respectivos titulares.
Referencias bibliográficas
- Este producto está destinado para el uso diagnóstico in vitro (in vitro diagnostic [IVD]).
- American Cancer Society. Aproximadamente el 60 % de los casos de carcinoma pulmonar diagnosticados en los Estados Unidos se realizaron en etapas avanzadas de la enfermedad. Un 5 % de los pacientes con CPNM en los Estados Unidos son ALK positivos. El CPNM ALK positivo suele presentarse en pacientes jóvenes sin antecedentes, o con antecedentes leves, de tabaquismo.
- van der Wekken AJ, Pelgrim R, ‘t Hart N, Werner N, Mastik MF, et al. Dichotomous. ALK-IHC is a better predictor for ALK inhibition outcome than traditional ALK-FISH in advanced non-small cell lung cancer. Clinical Cancer Research, 2017, 23(15):4251-4258. doi: 10.1158/1078-0432.CCR-16-1631.
- Zhou J, Zhao J, Sun K, Wang B, Wang L, et al. Accurate and economical detection of ALK positive lung Adenocarcinoma with semiquantitative immunohistochemical screening. PLoS ONE 2014, 9(3): e92828.doi:10.1371/journal.pone.0092828.
- Shan L, Lian F, Guo L, Yang X, Ying J, et al. Combination of conventional immunohistochemistry and qRT-PCR to detect ALK rearrangement. Diagnostic Pathology 2014, 9:3.doi:10.1186/1746-1596-9-3.
- Ying J, Guo L, Qiu T, Shan L, Ling Y, et al. Diagnostic value of a novel fully automated immunochemistry assay for detection of ALK rearrangement in primary lung adenocarcinoma. Annals of Oncology, 2013, 24(10):2589-2593; doi:10.1093/annonc/mdt295.
- La prueba aprobada ALK (D5F3) utilizada con el dispositivo de detección y amplificación OptiView DAB es una prueba totalmente automatizada que dura 4,5 horas. Su tinción puede realizarse junto con otras pruebas habituales de IHQ para obtener los resultados el mismo día y cumplir con las directrices actuales de CAP/IASLC/AMP para la utilización de pruebas de pacientes con carcinoma pulmonar. Lindeman NI, Cagle PT, Beasley MB, Chitale DA, Dacic S, et al. Directrices de pruebas moleculares para la selección de pacientes con carcinoma pulmonar para los inhibidores de tirosina cinasa del EGFR y ALK: directrices del College of American Pathologists, International Association for the Study of Lung Cancer y Association for Molecular Pathology. Journal of Thoracic Oncology 2013; 8(7):823–859. doi: 10.1097/JTO.0b013e318290868f.
Para más información

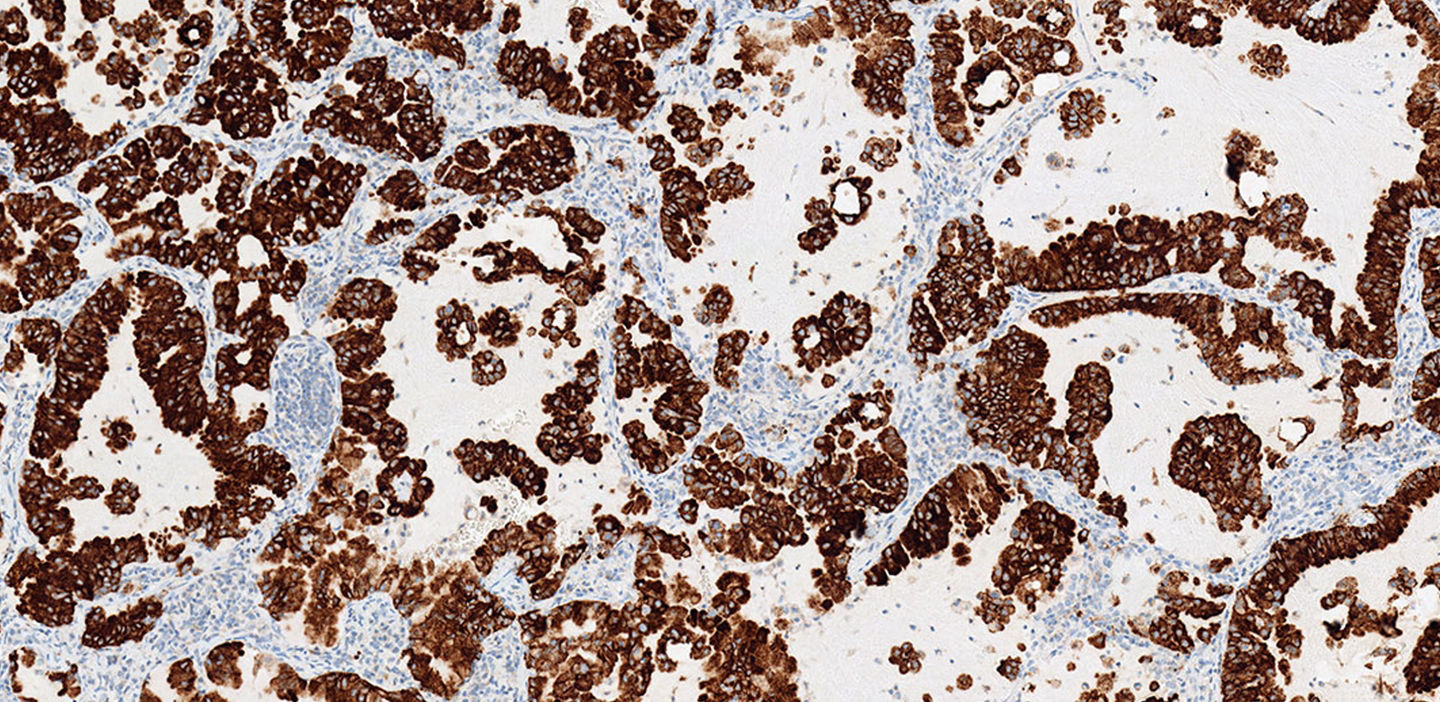
Tejido de carcinoma pulmonar no microcítico teñido con la prueba VENTANA ALK (D5F3) CDx y con y detección y amplificación OptiView DAB