Gabrielle Fimbres
responsable de comunicación externa
520.222.4573
[email protected]
El ensayo VENTANA PD-L1 (SP263) de Roche consigue ampliación del marcado CE para informar en la toma de decisiones terapéuticas en pacientes con cáncer de pulmón considerados para la inmunoterapia con KEYTRUDA (pembrolizumab).
Tucson (Arizona)
5 de mayo de 2017
- El carcinoma pulmonar sigue siendo la causa principal de muerte por cáncer, con casi 1,6 millones de muertes en el mundo.
- PD-L1 es una proteína implicada en la supresión del sistema inmunitario, lo que puede afectar a la capacidad del cuerpo para combatir el cáncer
- El ensayo VENTANA PD-L1 (SP263)1 está ahora disponible para países que aceptan el marcado CE para identificar a pacientes con cáncer de pulmón no microcítico metastásico (CPNMm) con y sin tratamiento previo elegibles para la inmunoterapia con KEYTRUDA.
Roche (SIX: RO, ROG; OTCQX:RHHBY) ha anunciado hoy el lanzamiento del ensayo VENTANA PD-L1 (SP263) como prueba de diagnóstico in vitro2 para KEYTRUDA® (pembrolizumab), un tratamiento anti-PD-1, para identificar a pacientes con cáncer de pulmón no microcítico metastásico (CPNMm) con y sin tratamiento previo elegibles para inmunoterapia. KEYTRUDA está comercializado por Merck & Co., Inc., Kenilworth, NJ, EE. UU., conocido como MSD fuera de EE. UU. y Canadá. El ensayo está disponible en países que aceptan el marcado CE.3
El cáncer de pulmón sigue siendo la causa principal de muerte por cáncer, con un 12,9 % anual estimado de todos nos nuevos casos de cáncer y casi 1,6 millones de muertes en el mundo. El CPNM representa aproximadamente el 85 % de todos los casos de cáncer de pulmón.4 Durante los últimos 30 años el cáncer de pulmón ha presentado la menor mejora en las tasas de supervivencia en comparación con otros cánceres.5
El ensayo VENTANA PD-L1 (SP263) es el único ensayo de PD-L1 totalmente automatizado para KEYTRUDA para su lanzamiento en la serie de instrumentos BenchMark de Roche. El lanzamiento debería aumentar de forma significativa el acceso de los pacientes a análisis de PD-L1 teniendo en cuenta la amplia base de instrumentos diagnósticos mundiales de Roche.
Roche lanzó por primera vez el ensayo VENTANA PD-L1 (SP263) en septiembre de 2016 como prueba diagnóstica para pacientes con CPNM metastásico previamente tratado en países que aceptan el marcado CE. Estamos encantados de ampliar esta aplicación para incluir a pacientes considerados para la inmunoterapia con KEYTRUDA como tratamiento de primera línea, afirmó Costello, jefa de Roche Tissue Diagnostics. El ensayo proporciona nuevas perspectivas sobre posibles opciones de tratamiento para esta enfermedad potencialmente mortal.
Roche seguirá buscando la aprobación normativa para el ensayo VENTANA PD-L1 (SP263) en otras indicaciones de cáncer y en otras localizaciones geográficas.
Acerca del ensayo VENTANA PD-L1 (SP263)
El ensayo VENTANA PD-L1 (SP263) ha sido diseñado para la detección cualitativa de la proteína del ligando de muerte programada 1 (PD-L1) en tejidos de carcinoma pulmonar no microcítico (CPNM) y otros tejidos tumorales fijados en formol e incluidos en parafina (FFPE) con tinción con el kit de detección de IHQ OptiView DAB en un dispositivo de tinción automatizada de la serie BenchMark.
La expresión de PD-L1 en la membrana de la célula tumoral (CT) detectada por la prueba VENTANA PD-L1 (SP263) en los tejidos de CPNM es una ayuda para la identificación de los pacientes aptos para el tratamiento con KEYTRUDA® (pembrolizumab).
La expresión de PD-L1 en la membrana de la célula tumoral (CT) detectada por la prueba VENTANA PD-L1 (SP263) en los tejidos de CPNM puede estar relacionada con una mejor supervivencia con el tratamiento con OPDIVO® (nivolumab).
Acerca de Roche
Roche es una empresa internacional, pionera en el desarrollo de medicamentos y productos de diagnóstico para hacer avanzar la ciencia y mejorar la vida de las personas. La potencia combinada farmacéutica y diagnóstica bajo un mismo techo ha convertido a Roche en el líder de la atención sanitaria personalizada, una estrategia orientada a proporcionar a cada paciente el mejor tratamiento posible.
Roche es la mayor empresa biotecnológica del mundo, con medicamentos auténticamente diferenciados en las áreas de oncología, inmunología, enfermedades infecciosas, oftalmología y enfermedades del sistema nervioso central Roche también es líder mundial en diagnóstico in vitro y diagnóstico de cáncer basado en el tejido, y se sitúa a la vanguardia en el control de la diabetes.
Fundada en 1896, Roche busca mejores vías de prevenir, diagnosticar y tratar las enfermedades, así como de contribuir al desarrollo sostenible de la sociedad. La empresa también tiene como objetivo mejorar el acceso de los pacientes a las innovaciones médicas trabajando con todas las partes interesadas pertinentes. La lista Modelo de Medicamentos Esenciales de la Organización Mundial de la Salud contiene 29 medicamentos desarrollados por Roche, entre ellos antibacterianos que salvan vidas, antipalúdicos y antineoplásicos. Por octavo año consecutivo, Roche ha sido reconocida en los Índices de Sostenibilidad Dow Jones (DJSI) como la empresa más sostenible del grupo Industria Farmacéutica, Biotecnología y Ciencias Biológicas.
El Grupo Roche, con sede central en Basilea (Suiza), está presente operativamente en más de 100 países y en el 2016, contaba con más de 94 000 empleados en todo el mundo. Ese mismo año, Roche invirtió 9900 millones de CHF en I+D y sus ventas alcanzaron la cifra de 50 600 millones de CHF. Genentech (Estados Unidos) es un miembro de plena propiedad del Grupo Roche. Roche es el accionista mayoritario de Chugai Pharmaceutical (Japón). Para más información, visita la página www.roche.com.
VENTANA, BENCHMARK y OPTIVIEW son marcas registradas de Roche. El resto de nombres de productos y marcas registradas son propiedad de sus respectivos titulares.
Referencias bibliográficas
- Este producto está destinado para el uso diagnóstico in vitro (in vitro diagnostic [IVD]).
- El ensayo VENTANA PD-L1 (SP263) ha demostrado equivalencia con el ensayo con marcado CE PD-L1 IHC 22C3 pharmDx, que ha demostrado previamente utilidad clínica a través de datos de KEYNOTE-024 y KEYNOTE-010. KEYNOTE-024 fue un ensayo de fase III, aleatorizado, abierto, controlado con fármaco activo y multicéntrico de 305 pacientes con CPNM metastásico sin tratamiento previo y cuyos tumores presentaron alta expresión de PD-L1 según una expresión tumoral de PD-L1 ≥50 % y sin aberraciones tumorales genómicas en EGFR o ALK. Los datos de los resultados demostraron supervivencia sin progresión y supervivencia global superiores en el tratamiento de primera línea del CPNMm con expresión de PD-L1 ≥50 %. KEYNOTE-010 fue un ensayo abierto, aleatorizado, controlado con fármaco activo, multicéntrico y de fase II/III de 1033 pacientes con CPNMm que habían progresado después de quimioterapia con platino y, si procede, tratamiento dirigido para aberraciones tumorales genómicas de EGFR o ALK. Se observó supervivencia global superior frente a docetaxel con una expresión de PD-L1 ≥1 %. Para un marcado CE, Roche se basó en un estudio de comparación de métodos llevado a cabo por AstraZeneca, en el que se comparan los datos ya disponibles de pruebas de PD-L1, DAKO pharmDx 22C3 (utilizada en los estudios clínicos de KEYTRUDA), DAKO pharmDx 28-8(utilizada en los estudios clínicos de OPDIVO) y SP263.
- Consulte la disponibilidad y las restricciones a su representante local.
- Ferlay J, Soerjomataram I, Ervik M, et al. GLOBOCAN 2012 v1.0. Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 11. http://globocan.iarc.fr. Publicado el 12 del 12 de 2013. Actualizado el 9 del 1 de 2014. Acceso el 8 del 2 de 2016.
- Siegel R, Naishadham D, Jemal A. Cancer Statistics, 2013. CA Cancer J Clin. 2013;63(1):11-30.
Para más información

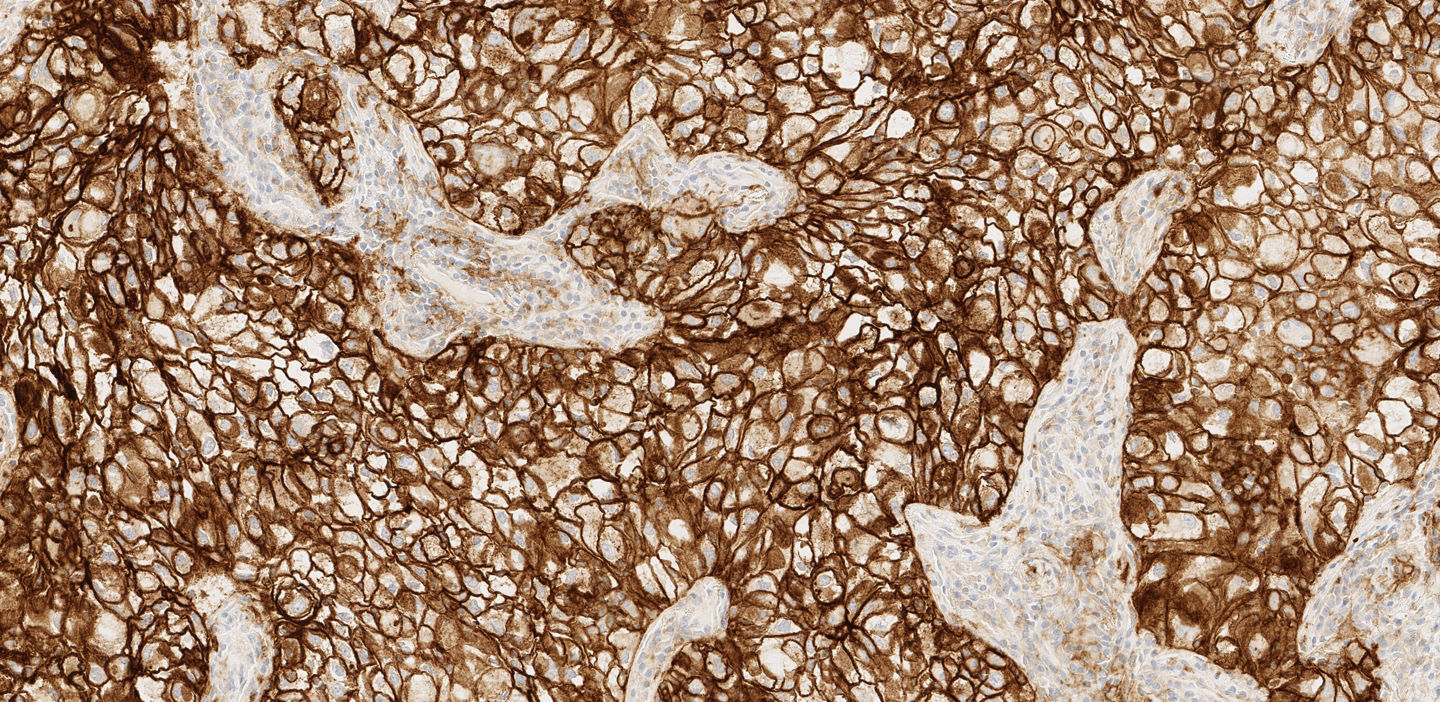
Ensayo VENTANA PD-L1 (SP263): tinción en cáncer de pulmón no microcítico (CPNM) con tinción membranosa y citoplasmática de las células tumorales