ベンタナ OptiView PD-L1 (SP263)

免疫療法における適切な
体外診断用医薬品としての承認
非小細胞肺癌(NSCLC)
非小細胞肺癌(NSCLC)においてアテゾリズマブ(遺伝子組換え)又はデュルバルマブ(遺伝子組換え)の投与判断の補助として承認されています。
対象疾患および適応
- 非小細胞肺癌の術後補助療法としてアテゾリズマブの投与を行う場合には、投与前にPD-L1発現率を確認する必要があり、コンパニオン診断薬として「ベンタナ OptiView PD-L1(SP263)」が承認されています。(医薬品の適応などに関する詳細については、アテゾリズマブの添付文書等を参照ください。)
- デュルバルマブの最適使用推進ガイドラインでは、PD-L1の発現率も確認した上で投与可否を判断することが望ましいとされています。(医薬品の適応などに関する詳細については、デュルバルマブの添付文書等を参照ください。)
ベンタナ OptiView PD-L1 (SP263)は、デュルバルマブの臨床試験において開発当初から使用されている検査法です。
関連情報
参考文献
1. Antonia SJ, et al. Durvalumab after Chemoradiotherapy in Stage III Non-Small-Cell Lung Cancer. N Engl J Med. 2017 Nov 16;377(20):1919-1929.
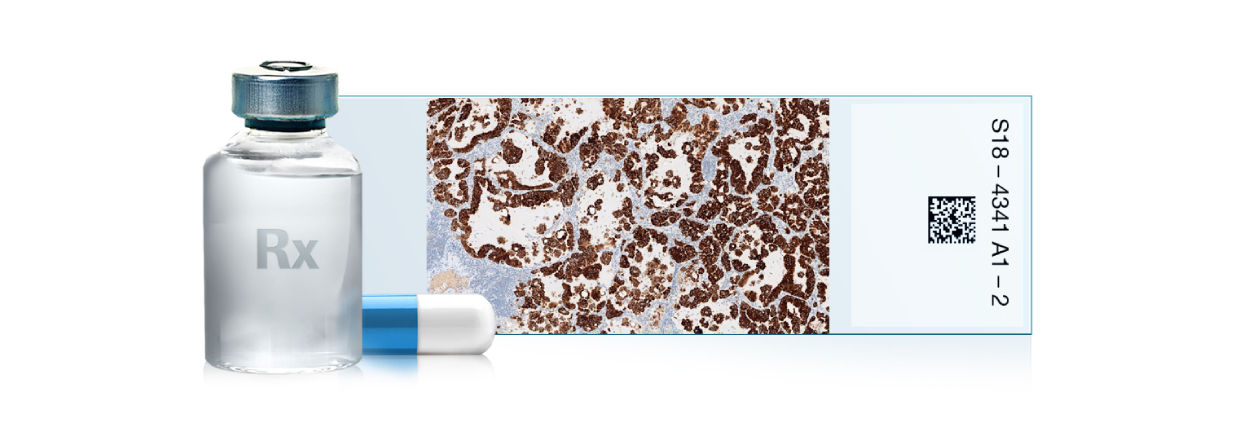
ベンタナ OptiView PD-L1 (SP263)は、ホルマリン固定パラフィン包埋標本において、免疫組織化学染色法によりがん組織又は細胞中のPD-L1発現率の測定を行う体外診断用医薬品として承認を受けています。
非小細胞肺癌(NSCLC):
非小細胞肺癌の術後補助療法としてアテゾリズマブ(遺伝子組換え)を投与する場合には、投与に先立ってPD-L1発現を確認することが必須となっており、「ベンタナ OptiView PD-L1(SP263)」がコンパニオン診断薬として承認されています。また、デュルバルマブのデュルバルマブの最適使用推進ガイドラインでは、PD-L1の発現率も確認した上で投与可否を判断することが望ましいとされています。
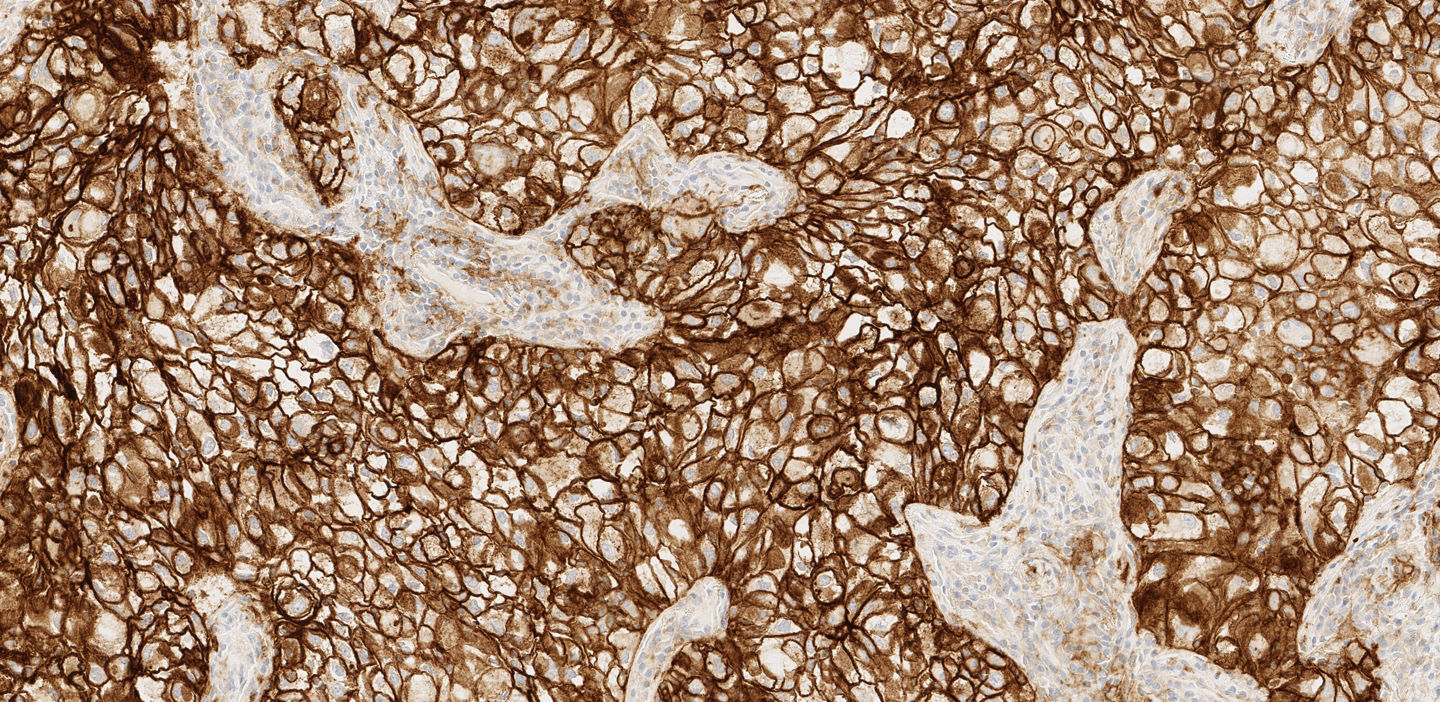
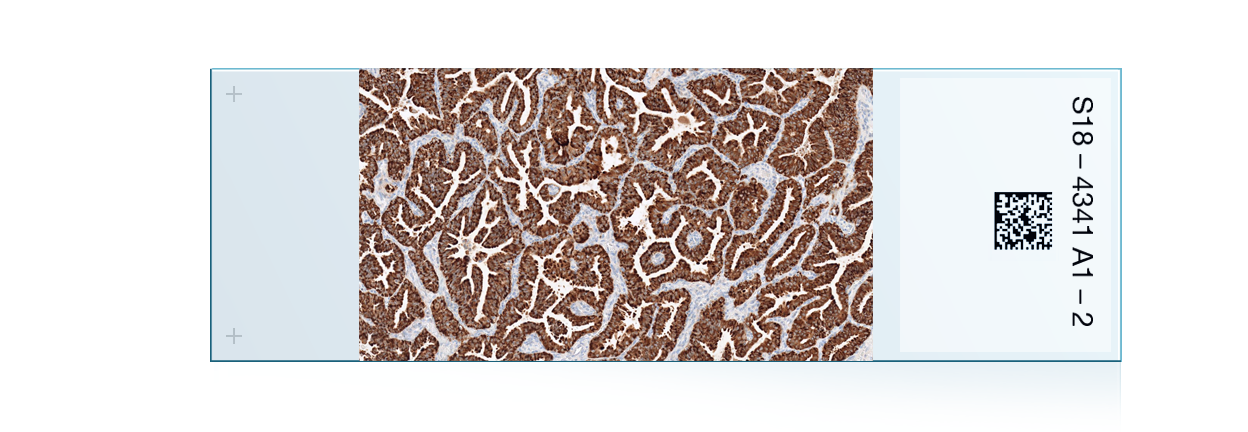
ベンタナ OptiView PD-L1 (SP263)による免疫染色は、細胞膜および細胞質に発現が認められますが、腫瘍細胞における細胞膜への染色性のみを評価します。
腫瘍細胞全体に対して、染色強度にかかわらず(但し、試薬対照スライドのバックグラウンド染色よりも強い染色強度)細胞膜への茶褐色の陽性反応が認められる腫瘍細胞の割合を算出し、腫瘍細胞におけるPD-L1発現率とします。
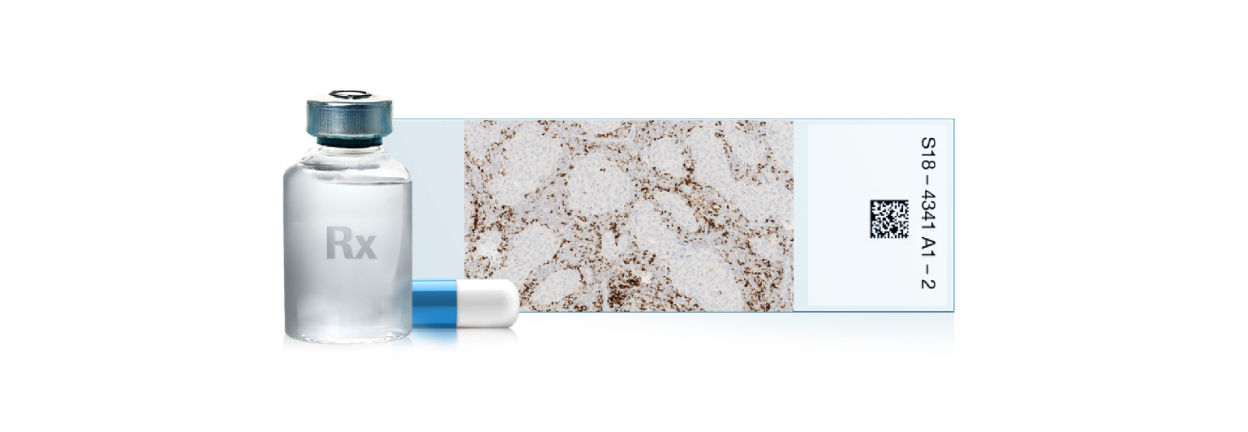
腫瘍細胞の細胞質や免疫細胞等にも発色が認められる場合がありますが、判定対象とはなりません。
詳しくは、弊社が提供する添付文書および検査ガイドを参照ください。
この製品は体外診断用医薬品として承認を受けています。
病理検査関連製品カタログ
E-Bookでロシュの製品ラインアップカタログ「病理検査関連製品カタログ」をご覧いただけます。
画面下のツールメニューからキーワード検索や拡大縮小機能などをご利用ください。
※お使いの環境によっては開かない、または、正常に動作しないことがございます。また、履歴の消去などのブラウザ側の動作によりメモや付箋は失われる可能性がございます。

文書・資料検索サイトeLabDoc
eLabDocは、ロシュ製品に関する文書や資料の検索サイトです。製品番号、ロット番号、製品名から、SDS、試験成績書(CofA)、英文添付文書を検索、閲覧することができます。
※eLabDocはRoche DiaLogのe-サービスの一つです。
eLabDocの情報の一部の取得にはRoche DiaLogへのログインが必要な場合があります。 Roche DiaLogはロシュユーザー向けのポータルサイトで、ご利用前に弊社社員を介した会員登録が必要です。別途お問い合わせください。
※体外診断用医薬品としての添付文書(日本語)についてはPMDAサイトから検索してください。