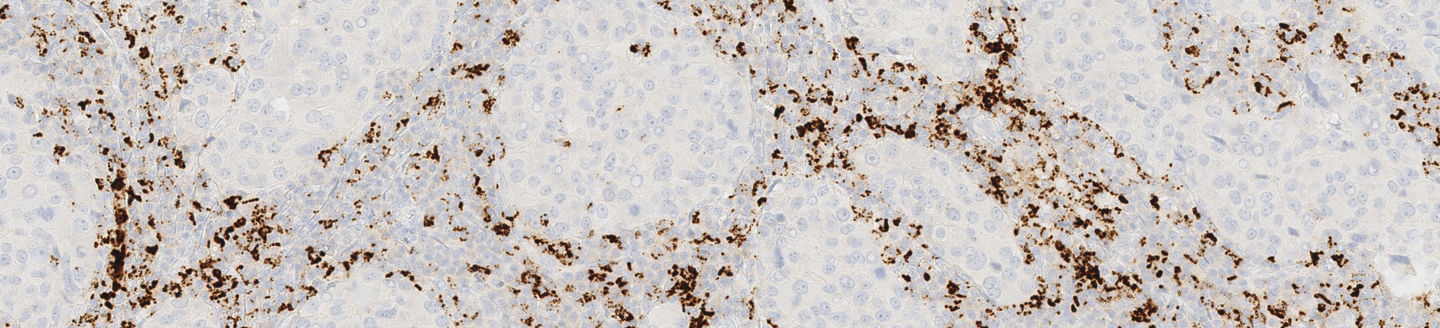
I test predittivi VENTANA PD-L1 identificano i pazienti che hanno maggiori probabilità di rispondere a immunoterapie specifiche garantendo risultati affidabili.
Test VENTANA PD-L1 (SP142) (CE IVD)

Fornire risposte ai patologi su PD-L1
Il test VENTANA PD-L1 (SP142)* garantisce la sicurezza per:
- Identificare i pazienti con carcinoma mammario triplo negativo (TNBC) idonei al trattamento con TECENTRIQ® (atezolizumab)
- Selezionare i pazienti affetti da carcinoma uroteliale (UC) idonei al trattamento con TECENTRIQ® (atezolizumab)
- Selezionare i pazienti con carcinoma polmonare non a piccole cellule (NSCLC) idonei al trattamento con TECENTRIQ® (atezolizumab)
* VENTANA PD-L1 (SP142) Assay potrebbe non essere disponibile per alcune indicazioni e/o limiti in tutte le aree geografiche. In Svizzera TECENTRIQ è approvato solo per il cancro del polmone non a piccole cellule.
Foglio illustrativo VENTANA PD-L1 (SP142) Assay.
Approvazione come Companion diagnostics
Carcinoma mammario, uroteliale e carcinoma polmonare non a piccole cellule.
È importante usare il test giusto per determinare lo stato di PD-L1 per le opzioni di immunoterapia. Il test VENTANA PD-L1 (SP142)* è il primo e l’unico test marcato CE-IVD per TECENTRIQ nei pazienti con carcinoma mammario, uroteliale (UC) e carcinoma polmonare non a piccole cellule (NSCLC). Questo test valuta l’espressione delle cellule colorando le cellule immunitarie fornendo informazioni che possono orientare le decisioni terapeutiche.
Test VENTANA PD-L1 (SP142):
- Il primo e l’unico test per PD-L1 clinicamente dimostrato come in grado di identificare i pazienti idonei per TECENTRIQ che presentano maggiori probabilità di trarre beneficio dall’utilizzo del farmaco
Argomenti correlati
VENTANA PD-L1 (SP142) Assay è un’analisi immunoistochimica che utilizza un anticorpo primario monoclonale di coniglio, anti-PD-L1, per la valutazione della proteina Programmed Death-Ligand 1 (PD-L1) nelle cellule tumorali e nelle cellule immunitarie infiltranti il tumore nei tessuti fissati in formalina e inclusi in paraffina (FFPE), colorati con i kit OptiView DAB IHC Detection Kit e OptiView Amplification Kit sullo strumento BenchMark ULTRA.
Il test IHC VENTANA PD-L1 (SP142) è utilizzato per valutare l’espressione della proteina PD-L1 nelle cellule tumorali e nelle cellule dell’infiltrato immunitario.
Il test VENTANA PD-L1 (SP142) è indicato come ausilio nell’identificazione di pazienti per il trattamento con le terapie per i rispettivi cutoff elencati nella Tabella 1 in conformità con l’etichettatura del prodotto terapeutico approvato.
Tabella 1. Indicazioni del test VENTANA PD-L1 (SP142) come Companion diagnostics
Visualizza tabella completaTabella 1. Indicazioni del test VENTANA PD-L1 (SP142) come Companion diagnostics
| Indicazione per l’uso | Terapia |
Cutoff |
|---|---|---|
| Carcinoma uroteliale | TECENTRIQ |
≥ 5% IC |
| Carcinoma mammario triplo negativo (TNBC) |
≥ 1% IC |
|
| Carcinoma polmonare non a piccole cellule (NSCLC) | ≥ 50% TC o ≥ 10% IC |
Questo prodotto è indicato per l'uso diagnostico in vitro (IVD).
Foglio illustrativo VENTANA PD-L1 (SP142) Assay.