Gabrielle Fimbres
responsable de comunicación externa
520.222.4573
[email protected]
Roche ha anunciado que ha obtenido la autorización de la FDA para companion diagnostics para identificar a los pacientes con carcinoma pulmonar no microcítico ALK positivo.
Tucson (Arizona)
01 de junio de 2017
- El carcinoma pulmonar es la causa de más de 1,6 millones de muertes al año en todo el mundo.1
- La cinasa de linfoma anaplásico (anaplastic lymphoma kinase, ALK) es un importante biomarcador que se encuentra en el carcinoma pulmonar no microcítico (CPNM). Su detección e inhibición puede ayudar a reducir los tumores de algunos pacientes con ALK positivo.
- La prueba VENTANA ALK (D5F3) CDx2 identifica los pacientes con CPNM ALK positivo aptos para recibir un tratamiento con el fármaco de Novartis ZYKADIA® (ceritinib), a fin de aumentar las opciones de tratamiento actuales.
Roche (SIX: RO, ROG; OTCQX:RHHBY) ha anunciado hoy que ha obtenido la autorización de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) para el uso de la prueba VENTANA ALK (D5F3) CDx como companion diagnostic para identificar a los pacientes con carcinoma pulmonar no microcítico (CPNM) ALK positivos aptos para recibir un tratamiento con el fármaco de Novartis ZYKADIA (ceritinib). La prueba VENTANA ALK (D5F3) es la única prueba inmunohistoquímica (IHQ) que cuenta con la autorización de la FDA como companion diagnostic para el uso de ZYKADIA.
El carcinoma pulmonar sigue siendo la causa principal de muerte por cáncer, con más de 1,6 millones de muertes en el mundo cada año.1
Con la autorización de la FDA para ampliar el uso de la prueba VENTANA ALK (D5F3) CDx para determinar qué pacientes con carcinoma pulmonar son aptos para recibir ZYKADIA, ayudamos a los médicos y a sus pacientes a identificar nuevas opciones de tratamiento para el carcinoma pulmonar no microcítico, indicó Ann Costello, directora de Roche Tissue Diagnostics. Se trata de un nuevo ejemplo del compromiso continuo de Roche por seguir avanzando en los tratamientos habituales para los pacientes con carcinoma pulmonar y la medicina personalizada.
La prueba VENTANA ALK (D5F3) CDx está disponible para su uso con los dispositivos BenchMark de IHQ/HIS.
Acerca de la prueba VENTANA ALK (D5F3) CDx
La prueba VENTANA ALK (D5F3) CDx ha sido diseñada para la detección cualitativa de la proteína cinasa de linfoma anaplásico (ALK) en tejido de carcinoma pulmonar no microcítico (CPNM) fijado en formol e incluido en parafina (FFPE) con tinción con un dispositivo automatizado BenchMark XT o BenchMark ULTRA. Su uso está indicado como ayuda para la identificación de pacientes aptos para el tratamiento con XALKORI® (crizotinib) o ZYKADIA® (ceritinib).
Este producto debe ser interpretado por un patólogo cualificado, junto con un examen histológico, información clínica pertinente y los controles adecuados.
Este producto está destinado para el uso diagnóstico in vitro (in vitro diagnostic [IVD]).
Acerca de ZYKADIA
Para más información sobre ZYKADIA (ceritinib), visita www.hcp.novartis.com/products/zykadia/alk-nsclc/.
Acerca de Roche
Roche es una empresa internacional, pionera en el desarrollo de medicamentos y productos de diagnóstico para hacer avanzar la ciencia y mejorar la vida de las personas. La potencia combinada farmacéutica y diagnóstica bajo un mismo techo ha convertido a Roche en el líder de la atención sanitaria personalizada, una estrategia orientada a proporcionar a cada paciente el mejor tratamiento posible.
Roche es la mayor empresa biotecnológica del mundo, con medicamentos auténticamente diferenciados en las áreas de oncología, inmunología, enfermedades infecciosas, oftalmología y enfermedades del sistema nervioso central Roche también es líder mundial en diagnóstico in vitro y diagnóstico de cáncer basado en el tejido, y se sitúa a la vanguardia en el control de la diabetes.
Fundada en 1896, Roche busca mejores vías de prevenir, diagnosticar y tratar las enfermedades, así como de contribuir al desarrollo sostenible de la sociedad. La empresa también tiene como objetivo mejorar el acceso de los pacientes a las innovaciones médicas trabajando con todas las partes interesadas pertinentes. La lista Modelo de Medicamentos Esenciales de la Organización Mundial de la Salud contiene 29 medicamentos desarrollados por Roche, entre ellos antibacterianos que salvan vidas, antipalúdicos y antineoplásicos. Por octavo año consecutivo, Roche ha sido reconocida en los Índices de Sostenibilidad Dow Jones (DJSI) como la empresa más sostenible del grupo Industria Farmacéutica, Biotecnología y Ciencias Biológicas.
El Grupo Roche, con sede central en Basilea (Suiza), está presente operativamente en más de 100 países y en el 2016, contaba con más de 94 000 empleados en todo el mundo. Ese mismo año, Roche invirtió 9900 millones de CHF en I+D y sus ventas alcanzaron la cifra de 50 600 millones de CHF. Genentech (Estados Unidos) es un miembro de plena propiedad del Grupo Roche. Roche es el accionista mayoritario de Chugai Pharmaceutical (Japón). Para más información, visita la página www.roche.com.
VENTANA y BENCHMARK son marcas registradas de Roche. El resto de nombres de productos y marcas registradas son propiedad de sus respectivos titulares.
Referencias bibliográficas
1. Organización Mundial de la Salud
2. Este producto está destinado para el uso diagnóstico in vitro (in vitro diagnostic [IVD]).
Para más información

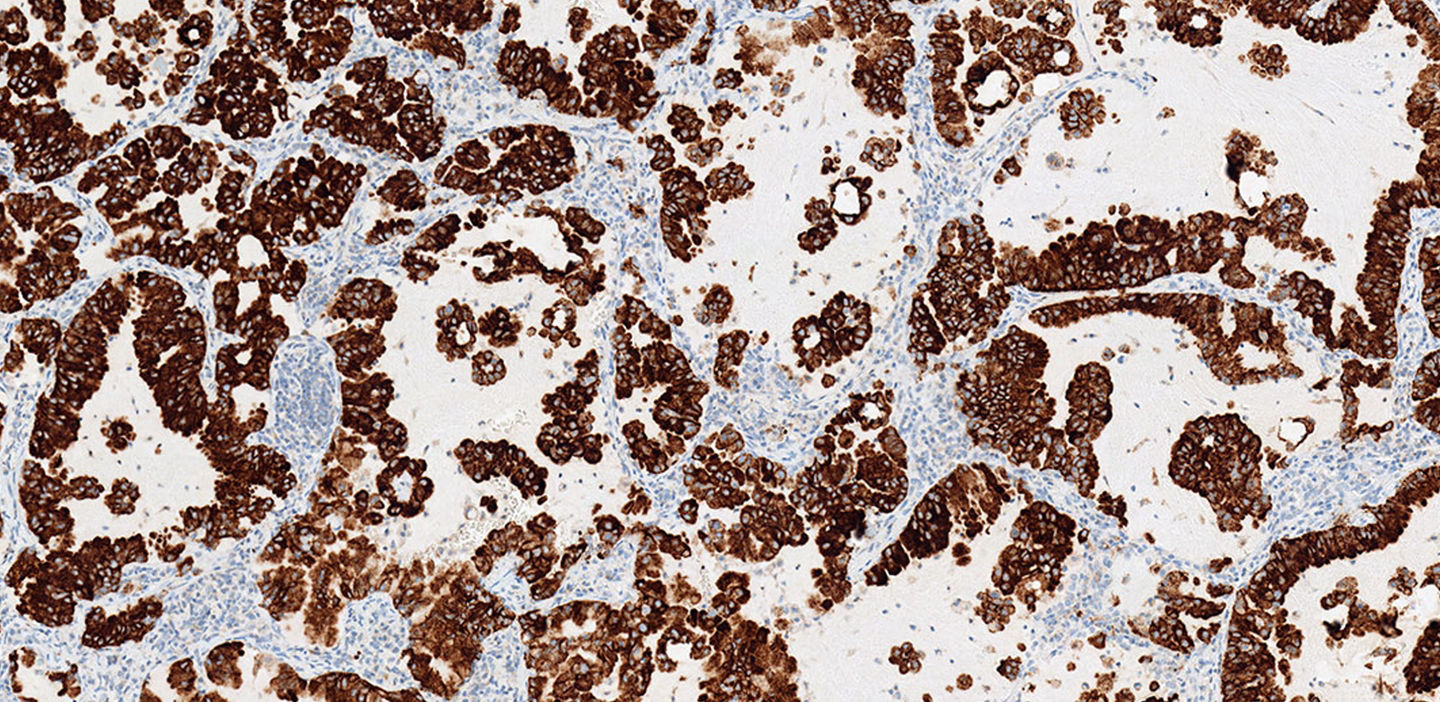
Tejido de carcinoma pulmonar no microcítico teñido con la prueba VENTANA ALK (D5F3) CDx y con y detección y amplificación OptiView DAB