
Case study: de zorg veranderen met digitale oncologie oplossingen

Het Marien-Hospital in het Duitse Wesel behandelt meerdere complexe oncologie-patiënten. Het ziekenhuis is gevestigd op één locatie met 16 verschillende medische afdelingen, ongeveer 432 bedden en 1.000 medewerkers. Elk jaar behandelt het ziekenhuis ongeveer 20.000 opgenomen patiënten en 50.000 poliklinische patiënten.1 In samenwerking met Roche onderzocht het Marien-Hospital het gebruik van digitale oncologische oplossingen om de patiëntzorg te verbeteren.
Overzicht
Nu we bewegen naar een digitale wereld waarin medische kennis exponentieel groeit2 is er dringende behoefte aan de vereenvoudiging en standaardisering van ziekenhuisprocessen zodat zorgprofessionals beschikbare data eenvoudig kunnen begrijpen en interpreteren.
Een uitdagend maar essentieel proces voor oncologische patiëntzorg is het management van tumor board meetings, waarin grote hoeveelheden gegevens van kankerpatiënten worden verwerkt en waarbij de input van meerdere specialisten nodig is om de optimale behandelaanbevelingen af te stemmen.
Wat verder bijdraagt aan de complexiteit zijn de vooruitgang van next-generation sequencing (NGS) en een toenemend aantal beschikbare mogelijkheden om kanker te behandelen, waardoor oncologie verder verschuift naar precisiegeneeskunde. Dit leidt tot toenemende behoefte aan en vorming van moleculaire tumor boards. 3, 4
In 2020 werkten zorgprofessionals van het Marien-Hospital samen met Roche Healthcare Consultants om een gestandaardiseerde en gedigitaliseerde moleculair tumor board workflow voor hun instituut in te richten. Voor dit project beschikte het ziekenhuis noch over een moleculair tumor board, noch over de kennis om dit innovatieve en complexe type tumor board te gebruiken.
Dankzij afstemming van mensen, processen en producten ontstond een gestandaardiseerde digitale workflow als gevolg van de samenwerking. Dit stelde zorgprofessionals in staat om een effectieve, patiëntgerichte moleculaire tumor board in te richten in het Marien-Hospital, waardoor verschillende complexe casusdata kunnen worden verwerkt, met weloverwogen, op wetenschap gebaseerde oncologische zorgbeslissingen als gevolg. Bovendien legde het de basis voor toekomstige veranderingen in gepersonaliseerde geneeskunde.
leestijd | 5 min
Blijf op de hoogte
Ontvang de meest recente inzichten uit de medische diagnostiek.

Het Marien-Hospital onderkende de absolute noodzaak om een moleculair tumor board in te richten. De samenwerking met Roche Healthcare Consulting genereerde transparante, data-gestuurde inzichten die de belangrijkste pijnpunten blootlegden in de voorbereiding, implementatie en nabeschouwing van de tumor boards. Deze inzichten vormden de basis in de bespreking over welke gebieden voorrang moeten krijgen. De belangrijkste geïdentificeerde kansen zijn:
Optimalisering van het management en de voorbereiding van tumor boards
Het beheer en de voorbereiding van multidisciplinaire tumor boards zijn een complex, tijd- en arbeidsintensief proces.5 Het vergt inspanning van meerdere zorgprofessionals om klinisch relevante data uit verschillende bronnen en gefragmenteerde IT-systemen te verzamelen, wat de administratieve lasten vergroot.5, 6
Het analyseren van complexe individuele genomische data maakt de voorbereiding op dit soort meetings uitdagender. Het gevolg is dat moleculaire tumor boards tot wel vier keer de voorbereidingstijd vergen vergeleken met een traditioneel tumor board.7
Standaardisering van tumor board processen
Momenteel bestaan er geen normen of richtlijnen voor moleculaire tumor board processen8,9 en geen gestandaardiseerde manier om patiënten te testen of hun gegevens te presenteren. De exponentiële groei van medische kennis maakt dit nog uitdagender voor clinici.2
Efficiëntieverbetering dankzij oncologische digitale oplossingen
Naast het stroomlijnen van workflows kunnen digitale oplossingen kosten verlagen, clinici ondersteunen met het nemen van weloverwogen beslissingen en uiteindelijk de kwaliteit van zorg verbeteren.10-12 Aanvullende hulp van digitale veranderingsconsultants, inclusief Roche Healthcare Consultants, kan bijdragen aan het herkennen van de belangrijkste zaken die moeten veranderen en het ondersteunen van zorgprofessionals tijdens en na de transitie naar een digitaal gerichte manier van werken.
Voordelen van de samenwerking van oncologieteams met adviseurs voor klinische besluitvorming zijn onder meer:
- Tijdsefficiëntere tumor board overleggen
- Verbeterde besluitvorming
- Toename dataconsistentie per tumor board case
- Toename tevredenheid werknemers
- Gestroomlijnde en gestandaardiseerde methoden voor de behandeling van patiënt cases
- Afname wachttijd behandeling patiënten
- Kwantitatieve vergelijking van entiteiten en moleculaire tumor boards
- Transparantie in personeelskosten
Benadering
Het Marien-Hospital had als algemeen doel om een virtueel netwerk van experts in precisie-oncologie te ontwikkelen en een digitale workflow-oplossing te implementeren, die het voeren van effectieve, patiëntgerichte tumor boards mogelijk maken. Bovendien hoopten ze dat hun werk zou leiden tot een grotere regionale zichtbaarheid en andere kleine ziekenhuizen in staat zou stellen om netwerken van experts op te zetten.
Samen met Roche Healthcare Consultants en geleid door een stuurgroep van het ziekenhuis vond een eerste ontmoeting plaats waarbij de teams gezamenlijk op één lijn kwamen wat betreft de vijf hoofddoelstellingen van dit project.
5 project-hoofddoelstellingen

- De wensen en behoeften van de zorgprofessional begrijpen
- Identificeer de incrementele waarde van iedere fase van de processen die bij het patiëntzorgtraject zijn betrokken
- Pijnpunten blootleggen en op maat gemaakte oplossingen ontwikkelen om deze op te lossen
- Samen workflow-standaarden creëren
- De juiste mensen samenbrengen en afstemmen op het proces en de implementatie van de cloud-based softwareoplossing
Een sequentiële benadering van het opzetten van moleculaire tumor boards
In het Marien-Hospital werd een sequentiële aanpak gebruikt voor de opzet van de moleculaire tumor boards. ‘Fase een: status quo’ werd uitgevoerd om de essentiële stappen in het proces te identificeren en het kader van de moleculaire tumor boards te bepalen voor de voorbereiding, implementatie en nabeschouwing van de vergaderingen. Afstemming van het procesontwerp vond plaats in ‘Fase twee: toekomstige staat’ en de laatste fase, ‘Fase drie, proefdraaien’, omvatte fijnslijpen en testen van de workflow.
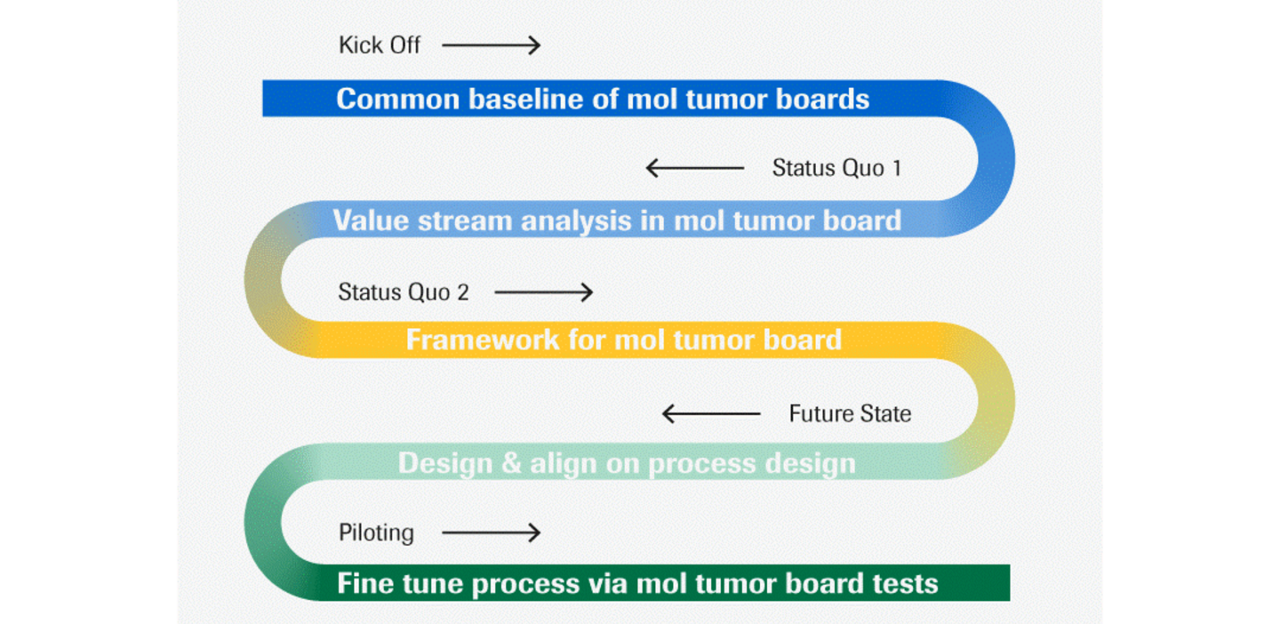
- Kick-off
Gemeenschappelijke basislijn mol. tumor boards - Status quo 1
Waardestroom-analyse in mol. tumor board - Status quo 2
Kader voor mol. tumor board - Toekomstige staat
Ontwerpen en afstemmen op procesontwerp - Proefdraaien
Fijnslijp proces via mol. tumor board tests
Uitkomsten
Als gevolg van het project werd een Duitsland-breed netwerk van experts in precisie-oncologie gecreëerd, samen met een gestandaardiseerde en gedigitaliseerde moleculaire tumor board workflow. Dit netwerk van experts en gestroomlijnde workflow faciliteerden al de implementatie van moleculaire tumor boards in het Marien-Hospital.
Het virtuele netwerk, dat bestaat uit tien partners en zeven klinische oncologische experts van zes instituten, ging live in juni 2020. Het eerste moleculaire tumor board werd in augustus 2020 gehouden.
Na het opzetten van het netwerk van experts en de gestroomlijnde workflow zijn moleculaire tumor boards gehouden die resulteerden in:

- Hoge investeringen in middelen (ongeveer € 600 investering per lid) per moleculair tumor board
- Zeer complexe patiëntgevallen: gemiddeld 14 minuten overleg
- Gebruik van meerdere databronnen voor een holistische kijk op ieder geval (inclusief CT-scans, klinische proeven, experimentele proeven, biomarkers, whole genome sequencing resultaten)
- Duitsland-brede topspecialisten voor specifieke entiteiten dragen virtueel bij aan relevante gevallen om het kernnetwerk te ondersteunen met hun expertise
- Wanneer nodig worden specialisten ook voordat tumor boards plaatsvinden geconsulteerd om hun feedback betreft complexe patiëntgevallen te verzamelen
Conclusies
Digitale hulpmiddelen, zoals opkomende technologieën voor klinische besluitvorming, bieden de mogelijkheid om de efficiëntie van moleculaire tumor boards te verbeteren.5,13,14 Naast het stroomlijnen van workflows kunnen digitale oplossingen kosten verlagen, clinici ondersteunen met het nemen van weloverwogen beslissingen en uiteindelijk de kwaliteit van ontvangen zorg verbeteren, zoals aangetoond in onderzoeken.10-12 Extra ondersteuning door digitale transformatie-consultants kan bijdragen aan het identificeren van de belangrijkste factoren die verandering behoeven en zorgprofessionals helpen tijdens en na de transitie naar een digitaal gerichte manier van werken.
Het project in het Marien-Hospital toont aan dat voor de succesvolle implementatie van gestandaardiseerde moleculaire tumor board workflows samenwerking nodig is tussen digitale gezondheidszorg consultant experts, hoogwaardige digitale oplossingen en betrokken zorgmedewerkers die de toekomst van de zorg voor hun oncologische patiënten willen veranderen.
Referenties
- Marien-Hospital Wesel. (2021). Article available from https://prohomine.de/marien-hospital-wesel/ [Accessed May 19, 2021]
- Densen P. (2011). Transactions of the American Clinical and Climatological Association 122, 48–58
- Malone et al. (2020). Genome Medicine 12, 8
- Madhavan et al. (2018). American Society for Clinical Oncology Educational Books 38, 546–553
- Krupinski et al. (2001). Journal of Pathology Informatics 9, 26
- Knaup et al. (2001). Methods of Information in Medicine 40, 90–98
- Internal Analysis: Momentum: Molecular Tumor Boards, Roche Healthcare Consulting, 2020
- van der Velden et al. (2017). Annals of Oncology 28, 3070–3075.
- Rieke et al. (2018). JCO Precision Oncology 2, 1–14
- Menachemi et al. (2011). Risk Management Healthcare Policy 4, 47–55
- Patkar et al. (2011). International Journal of Breast Cancer, 831605
- Nardi et al. (2016). Journal of the National Comprehensive Cancer Netwwork 14, 1226–1233
- Fowler et al. (2019). Journal of Clinical Oncololgy 37(15_suppl), e18028
- Hammer et al. (2020). JCO Clinical Cancer Informatics 4, 757–768